|
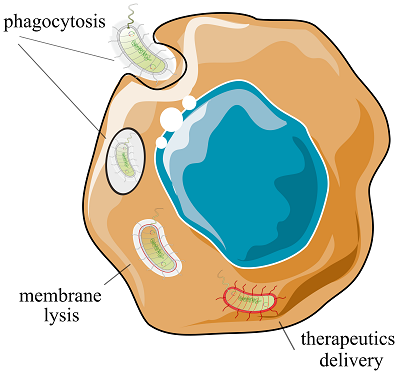
СОДЕРЖАНИЕ 1. БАКТЕРИАЛЬНЫЙ «ФРАНКЕНШТЕЙН»: КАК СДЕЛАТЬ ДОБРОГО ДОКТОРА ИЗ ЗЛОГО МИКРОБА. 2. БАКТЕРИЯ-РОБОТ СПЕШИТ НА ПОМОЩЬ: УПРАВЛЕНИЕ И ДОСТАВКА 3. ВООРУЖЕННЫЙ ДО ЗУБОВ: ТЕРАПЕВТИЧЕСКИЙ И ДИАГНОСТИЧЕСКИЙ ПОТЕНЦИАЛ БАКТЕРИАЛЬНОГО РОБОТА 5. БАКТЕРИАЛЬНЫЙ РОБОТ... БЕЗ БАКТЕРИИ: ПЕРСПЕКТИВЫ СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ Рисунок 5Инвазия бактерии внутрь раковой клетки для высвобождения терапевтического груза. Таблица 1Различные стратегии модификации бактерий. Таблица 2Принципы разработки бактериального робота для терапии рака. Таблица 3Биологические носители в создании бактериального робота. |
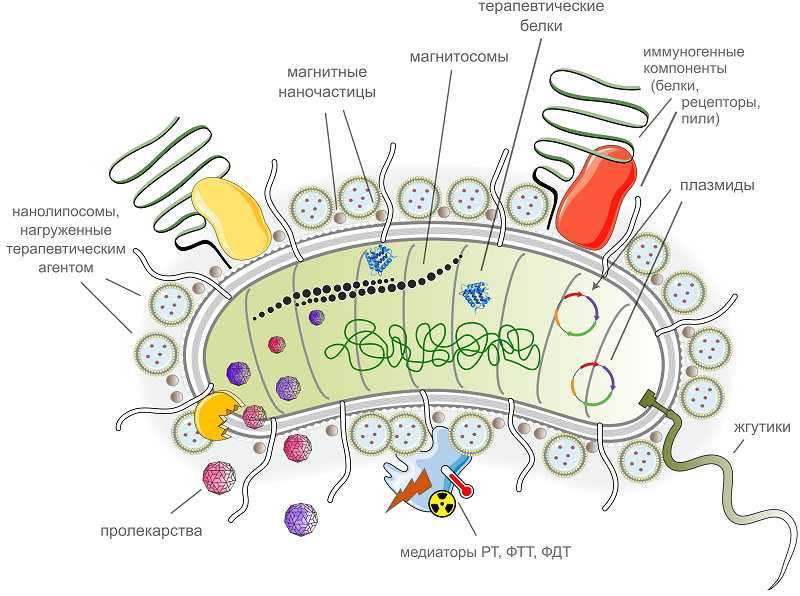
БАКТЕРИОБОТЫ: БАКТЕРИАЛЬНЫЕ МИКРОРОБОТЫ И ИХ ПОТЕНЦИАЛ В ДИАГНОСТИКЕ И ТЕРАПИИ РАКА Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский университет), 119991 Москва, Россия; *e-mail: larisa.ikryannikova@gmail.com Ключевые слова: бактериальный микроробот; бактериобот; бактериальный биогибрид; противоопухолевая терапия DOI: 10.18097/BMCRM00301 ВВЕДЕНИЕ Онкологические заболевания представляют собой одну из серьезнейших проблем общественного здравоохранения во всем мире, унося более десяти миллионов жизней ежегодно. Несмотря на значительные усилия в разработке способов борьбы с раком, современные клинические методы лечения онкологий все еще имеют ряд ограничений - серьезные побочные эффекты, ограниченная эффективность при метастазировании и рецидивах, высокая стоимость лечения каждого пациента. Поэтому разработка новых терапевтических подходов в онкологии имеет важнейшее и приоритетное значение [1]. Понятие «бактериобот» - бактериальный микроробот - появилось в терминологии научного пространства относительно недавно. Впервые этот термин был введен, вероятно, в работах Park 2013-2014 гг. для обозначения новой инновационной тераностической методологии изготовления препаратов на основе бактерий для терапии злокачественных опухолей [2-3]. Идея использовать бактерии в качестве терапевтического средства имеет под собой основание: бактерии представляют собой универсальный и пластичный природный биоматериал, который обладает свойством самостоятельно передвигаться и, при определенных условиях, проникать в самые труднодоступные опухолевые ткани, что крайне важно для решения вопроса доставки терапевтических агентов. Помимо этого, бактерии обладают естественной иммуногенностью, что позволяет повысить эффективность противоопухолевой иммунотерапии [4-6]. Бактериобот представляет собой конструкцию, включающую микросенсор для обнаружения злокачественных клеток, микроактуатор – для достижения мишени, и терапевтический агент для лечения [2]. Бактериоботом можно было бы назвать любую бактерию, которая была тем или иным образом намеренно модифицирована, например, при помощи генно-инженерных методов; однако в научной литературе, по-видимому, утверждается в настоящее время более узкое представление о бактериальном роботе как об объекте, объединяющем нативные или генно-модифицированные бактерии или части бактерий с синтетическими нано- и микроразмерными материалами и структурами [7-12]. История "использования" бактерий в противоопухолевой терапии уходит корнями в глубокое прошлое. Взаимосвязь между бактериальными инфекциями и лечением “опухолей”, которые, вполне возможно, представляли собой раковые ткани, была задокументирована египетским врачом Имхотепом более трех тысяч лет назад [13-14]. Наблюдения, описывающие факты регрессии злокачественной опухоли у людей, подвергшихся бактериальному заражению, упоминались в медицинских документах первой трети 19 века [15]. Широко известен и вошел в учебники случай, описанный в 1860-х годах немецким врачом В. Бушем, когда пациентка с раком неизвестной этиологии была намеренно инфицирована помещением в койку, в которой другой пациент недавно умер от рожистого воспаления - заболевания, вызываемого пиогенным стрептококком (Streptococcus pyogenes). Как и ожидалось, произошло заражение, при этом опухоль действительно начала регрессировать, но пациентка вскоре умерла от стрептококковой инфекции [13, 16-17]. Несколько позже возникла т.н. инфекционная теория канцерогенеза, которая связывала образование и распространение опухолей с бактериальными или паразитарными инфекциями. В то время, в конце 19 – начале 20 вв., многие исследователи и врачи пытались найти «cancer germ» - микробный агент, вызывающий рак, и доказать его роль в онкогенезе [18-21]. Одновременно имели место попытки разработать первые противоопухолевые “вакцины” на основе инактивированных или ослабленных бактерий. Одним из ярких примеров может служить препарат, известный под названием «токсины Коули» (“Coley’s toxins”). Этот препарат был разработан в начале 20-го века хирургом В. Коули, отметившим регрессию опухолей у своих пациентов с костной саркомой в случае инфицирования раневой поверхности после хирургического вмешательства, и представлял собой смесь инактивированных нагреванием бактерий S. pyogenes и Serratia marcescens [22-24]. Часто исследователи пытались создать противоопухолевые вакцины на основе тех микроорганизмов, которые они наблюдали – или полагали, что наблюдают – микроскопически внутри образцов ткани опухолей или в крови онкологических пациентов [16, 18, 25-26]. Несмотря на значительные усилия и отдельные успехи, создать универсальную, эффективную и надежную вакцину «против рака» на основе микроорганизмов так и не удалось. Как результат, теория бактериального (паразитарного) онкогенеза, популярная на рубеже 19 и 20 вв, к середине прошлого столетия была в целом отвергнута научным и медицинским сообществами, и почти забыта. Информация, накопленная за более чем сто лет, оставалась практически невостребованной, когда в конце 20-го века в научном мире произошли два значительных события. Во-первых, была установлена - или, скорее, официально признана - этиологическая роль Helicobacter pylori в развитии рака желудка [27]. Помимо H. pylori, есть и другие, пусть пока и не признанные официально, «претенденты на главную роль» в отдельных онкопроцессах. Так, Bacteroides fragilis, Streptococcus bovis и Fusobacterium nucleatum прочно ассоциируются с колоректальным раком, Chlamydia trachomatis - с раком шейки матки, а Porphyromonas gingivalis - с онкологическими заболеваниями ротовой полости [28-30]. Во-вторых, произошел резкий качественный скачок в развитии молекулярно-биологического инструментария, дающий, в числе прочего, возможность изучения таксономического состава микробных сообществ без стадии культивирования чистых бактериальных культур, что позволило приблизиться к пониманию «микробиома» злокачественных опухолей и его возможной роли в онкогенезе. Возрождению идеи использования микробов в борьбе с онкологическими заболеваниями способствовало также стремительное усовершенствование методов генной инженерии, в частности, методов редактирования генома. Если сто лет назад исследователи пытались создавать первые противоопухолевые «вакцины» на основе природных, нативных бактерий, в лучшем случае лишенных свойств вирулентности посредством многократного пассирования штамма, то современные «бактериальные» онкопрепараты представляют собой, без преувеличения, произведения генно-инженерного искусства, где из бактериальной клетки удалены факторы вирулентности, усилены свойства иммуногенности и многократно увеличена специфичность к опухолевым клеткам. Некоторые бактериальные филумы, такие как Clostridia, Salmonella или Listeria, привлекли особое внимание исследователей благодаря тому, что эти бактерии анаэробны и достаточно инвазивны для того чтобы проникать в гипоксические очаги внутри солидных («твердых») опухолей и существовать в них какое-то время. Препараты, разработанные на основе генно-модифицированных штаммов этих бактерий, в настоящее время находятся на разных стадиях клинических исследований [31-35]. Последним и решающим шагом к созданию бактериального робота стало развитие технологий работы с микро- и наноразмерными объектами. По-видимому, комбинация нанотехнологических разработок с биологическими носителями представляет собой наиболее многообещающую стратегию для преодоления физиологических барьеров (гематоэнцефалического барьера, гипоксических очагов внутри опухоли) и адресной доставки терапевтических агентов [36]. Химически, физически, биологически модифицированные бактерии, недоступные для распознавания иммунной системой человека вне опухоли, вооруженные терапевтическими средствами и нацеленные точно на раковые клетки, становятся настоящими роботами-полицейскими на службе по охране здоровья человека. Именно такие бактериальные роботы – способы их создания, нацеливания на мишень и снабжения терапевтическими грузами – и находятся в фокусе настоящего обзора. 1. БАКТЕРИАЛЬНЫЙ «ФРАНКЕНШТЕЙН»: КАК СДЕЛАТЬ ДОБРОГО ДОКТОРА ИЗ ЗЛОГО МИКРОБА Итак, бактериобот – это миниатюрное устройство на основе бактерий или частей бактерий, объединяющее в себе функции 1) сенсора для обнаружения мишени, 2) терапевтического агента или контейнера для переноса терапевтических средств, и 3) актуатора (исполнительного механизма), который направляет это устройство к месту назначения и запускает его работу (рис. 1) [37]. Подобное устройство может быть сконструировано при помощи биологических, химических или физических методов [6, 38-40] и содержать только компоненты клеточного производства, или же представлять собой биогибрид как клеточных, так и синтетических – биосовместимых и биоразлагаемых – компонентов неорганической природы.
Под биологическими методами подразумеваются прежде всего методы генной инженерии бактерий. Стремительное развитие в последние десятилетия генетических технологий, в частности, платформ высокопроизводительного секвенирования, привело к накоплению информации о структуре бактериальных геномов, что, в свою очередь, позволило выявить большое количество функциональных генетических элементов и создать базу для конструирования генетически модифицированных бактерий. Видоизмененные бактерии наделяются способностью производить терапевтические препараты in situ непосредственно внутри опухоли или усиливать иммунный ответ организма. Значительная часть генно-инженерных модификаций направлена на снижение бактериальной вирулентности в целях безопасности для пациента, а также на повышение тропности к опухоли [10]. К настоящему моменту существует большое число примеров генетической модификации бактерий для использования в онкотерапии, детальное рассмотрение которых не является целью настоящей статьи. Мы ограничимся отсылкой к некоторым замечательным обзорам [11-12, 34, 41-44], отдельные примеры можно увидеть также в таблице 1.
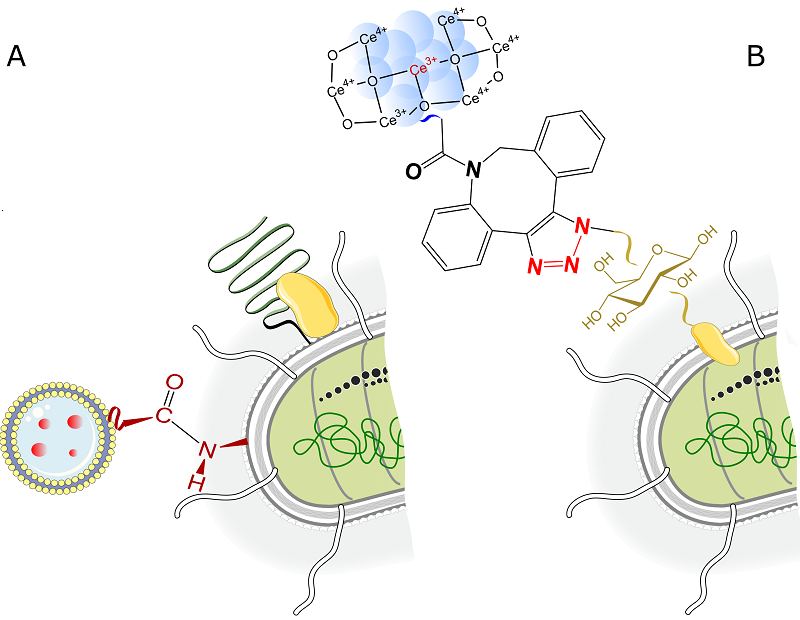
Под химическими методами модификации имеется в виду направленное прикрепление к бактерии различного рода биосовместимых и биоразлагаемых компонентов путем создания химических сшивок. Клеточная стенка бактерий состоит из пептидогликана – полисахаридного каркаса, образованного N-ацетилмурамовой кислотой и N-ацетилглюкозамином через β-1,4 гликозидные связи. Эта богатая аминогруппами и карбоксильными группами поверхность обеспечивает реакционные центры для химических сшивок. В работе Taherkhani [49] представлен пример ковалентного связывания бактерии Magnetococcus marinus с нагруженными лекарственным средством нанолипосомами для создания управляемой магнитотаксической бактериальной конструкции, способной двигаться при помощи внешнего магнитного поля. В основе создания биоконъюгата лежит карбодиимидный метод формирования амидной (пептидной) связи между активированными карбоксильными группами на поверхности нанолипосом и аминогруппами бактериальной стенки M. marinus (Рис. 2А). Аналогичным способом, за счет формирования амидной связи между карбоксилированными магнитными наночастицами (MNP-COOH) и поверхностью генетически модифицированного пробиотического штамма Escherichia coli Nissle 1917, получен биогибрид EcN@MNP, чувствительный к магнитному полю и пригодный для дальнейших модификаций [55]. Принципы карбодиимидной химии успешно применялись и для создания биогибридного комплекса на основе непатогенного штамма E. coli MG1655 с выраженной сверхпродукцией цитотоксического белка ClyA с наночастицами сульфида висмута (III) [56]. Наночастицы Bi2S3 (BNP) были связаны с бактериальной стенкой пептидным фрагментом, имитирующим субстрат матриксной металлопротеиназы-2 человека (MMP-2). Колонизация опухоли биогибридом E.coli@BNP сопровождалась деградацией пептидного фрагмента при помощи MMP-2, присутствующей в матриксе опухолевых клеток молочной железы, и высвобождением наночастиц Bi2S3, которые, как предполагается, повышают чувствительность к ионизирующему излучению в ходе лучевой терапии в результате генерации активных форм кислорода (АФК) [56]. Давно известный инструмент создания прочной и устойчивой нековалентной связи между фрагментами биогибридных конструкций в арсенале биотехнологов - стрептавидин-биотиновый комплекс. В работе [50] липосомы, нагруженные терапевтическим агентом паклитакселом, были пришиты к штамму Salmonella typhimurium за счет связывания стрептавидина, покрывающего поверхность липосом, с биотином на внешнемембранных белках бактерии. Похожим способом, с использованием биотин-стрептавидиновых сшивок, была сконструирована гибридная микроплатформа, состоящая из генно-модифицированного штамма E. coli MG1655, магнитных наночастиц для контроля движения и нанолипосом, нагруженных доксорубицином и фототермическим агентом индоцианиновым зеленым [57]. Говоря о методах химической инженерии бактерий, стоит упомянуть биоортогональную реакцию пары азид-циклооктин – сложный и красивый подход, предложенный в работе Pan [51] для создания бактериально-абиотического гибрида E. coli с наночастицами оксида церия (IV). Термином «биоортогональная реакция» принято обозначать химические процессы, которые могут протекать в физиологических условиях внутри клеток или живых организмов, не затрагивая естественные биохимические процессы в них. Субстрат 2-азидо-2-деокси-D-глюкоза был выбран в качестве источника сахара для культивирования бактерий для получения азида на клеточной стенке упомянутого выше штамма E. coli MG1655 (N3-Bac), в то время как оксид церия был модифицирован азо-дибензоциклооктином (DBCO), сформировав комплекс СеО2-DBCO. В дальнейшем, наночастицы оксида церия были заякорены на поверхности бактерии посредством биоортогональной клик-реакции между –DBCO и -N3 фрагментом (Рис. 2B). Модифицированная подобным образом бактерия предназначена для одновременной биоабсорбции катионов свинца и нейтрализации АФК в организме человека. Такой же способ применен авторами работы [58] для формирования химической связи между DBCO-модифицированными парамагнитными наночастицами Fe3O4 и генно-инженерным авирулентным штаммом E. coli BL21.
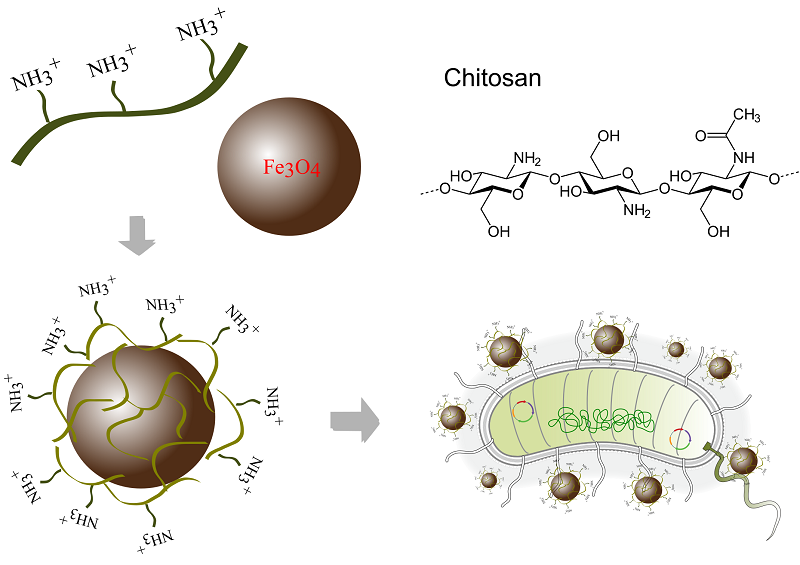
В качестве еще одного примера химической модификации бактерий можно привести создание бактериально-неорганических композитов на основе естественных процессов биоминерализации [59]. Биоминерализация, в широком понимании - это процесс образования твердых неорганических веществ внутри живого организма. Типичным примером природно биоминерализованных микроорганизмов являются упомянутые выше магнитотаксические (магнитотропные) бактерии, которые синтезируют магнитные наночастицы в собственной цитоплазме. Благодаря этому свойству, магнитотропные бактерии чувствительны к внешним магнитным полям и могут быть использованы, например, для визуализации опухолей или доставки терапевтических средств [60]. Природная способность к биоминерализации открывает интересные перспективы для создания биогибридов с интересующими свойствами. Так, в работе Wang и соавторов [61] были сконструированы гибридные фототермически активируемые бактерии на основе штамма E. coli MG1655. Бактериальный штамм был трансформирован плазмидой, содержащей ген цитотоксического пороформирующего белка цитолизина А (ClyA) с термочувствительным промотором; это позволило активировать экспрессию clyA тепловым воздействием. Далее бактерии культивировали совместно с тетрахлорзолотой кислотой H[AuCl4]. В процессе культивирования происходило восстановление H[AuCl4] на поверхности бактериальных клеток до наночастиц золота под действием бактериальной NADPH-редуктазы, с образованием термически активируемого биогибрида (ТАВ) - TAB@Au. Под воздействием лазерного облучения наночастицы золота нагревались и активировали экспрессию гена цитолизина для уничтожения опухолевых клеток [61]. Для создания биомиметических материалов с участием бактерий применяются металлоорганические соединения, например, цеолитоподобные имидазолатные каркасы (ZIF) с высокой сорбционной емкостью. Подобный подход использован авторами [62], где металлоорганический имидазолатный каркас ZIF-90, нагруженный метиленовым синим, был пришит к поверхности анаэробной бактерии Shewanella oneidensis MR-1 путем формирования иминогруппы в результате реакции аминогруппы поверхности бактерии с альдегидной группой металлоорганического соединения. Метиленовый синий, инкапсулированный в структуре ZIF-90, при освещении продуцирует синглетный кислород (1О2) в опухолевых клетках, провоцируя дисфункцию митохондрий и способствуя ингибированию синтеза АТФ и подавлению экспрессии генов белков теплового шока. В работе Yan и соавторов [53] был сконструирован композит на основе штамма E. coli MG1655 и имидазолатного каркаса ZIF-8, нагруженного фотосенсибилизатором (хлорин Е6) и цитостатическим препаратом доксорубицином, для комбинированной терапии опухолевых клеток. Биогибрид E.coli@ZIF-8/C&D формировался в результате химической реакции 2-метилимидазола с сульфатом цинка (II) в присутствии E. coli, хлорина Е6 (С) и доксорубицина (D), при этом захватившие фотосенсибилизатор и терапевтический агент частицы ZIF-8 равномерно распределялись по поверхности бактериальной клетки [53]. Среди физических методов модификации бактерий чаще всего используют электростатическое взаимодействие. В нормальных физиологических условиях клеточная стенка бактерий несет небольшой отрицательный заряд, что обеспечивает стабильный электростатический контакт с положительно заряженными наночастицами – например, частицами золота, функционализированного катионным полиэтиленимином с разветвленной структурой [63]. Показано, что прочность связывания золотых наночастиц с поверхностью грам-положительного штамма Bacillus subtilis зависит, в том числе, от доступности отрицательно заряженных фрагментов в тейхоевых кислотах клеточной стенки бактерии [63]. Для модификации магнитных наночастиц оксида железа предложено использовать хитозан - поликатионный биополимер с большим количеством аминогрупп в составе [64]. Модифицированные наночастицы эффективно связывались с бактериальной стенкой грам-отрицательной E. coli и грам-положительного золотистого стафилококка (рис. 3).
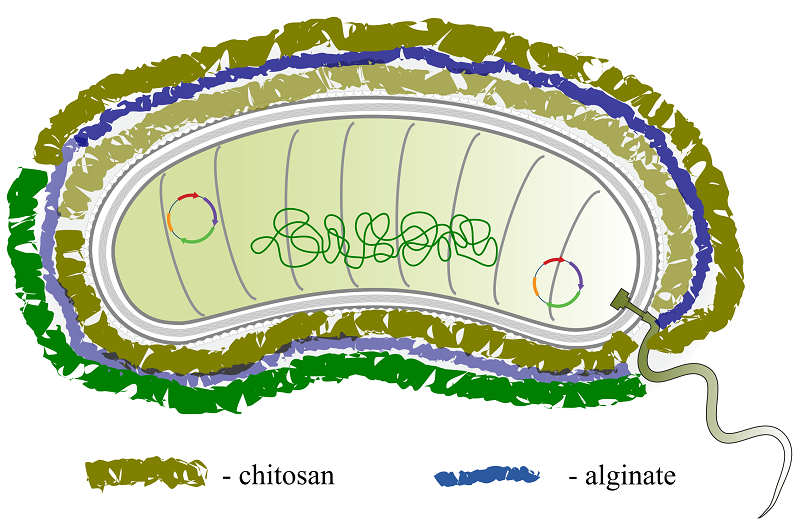
Стратегия "заряжения" бактерий при помощи нанофотокатализатора для усиления метаболической активности предложена в работе Zheng и соавторов [65]. Поверхность E. coli MG1655 была покрыта за счет сил электростатического притяжения нитридом углерода C3N4, легированным углеродными частицами (carbon-dot doped carbon nitride, CCN). Полученная конструкция CCN@E.coli предназначалась для фотоуправляемой терапии с использованием бактериальных метаболитов: световое воздействие стимулировало перенос фотоэлектронов от C3N4 на бактерию с последующим ферментативным преобразованием эндогенного нитрат-аниона до цитотоксического монооксида азота NO в зоне злокачественного новообразования. В исследовании Ding и соавторов [66] ультрамалые (3 нм) частицы черного фосфора (BPQDs, black phosphorus quantum dots) были электростатически адсорбированы на поверхности штамма E. coli Nissle 1917. Выбранный штамм был предварительно генетически модифицирован с целью увеличения продукции фермента каталазы. Частицы BPQDs характеризуются поглощением световой энергии в широком диапазоне длин волн и высокой эффективностью фототермического преобразования. Лазерное облучение биогибрида E.coli/BPQDs при 660 нм генерирует АФК, которые разрушают бактериальную мембрану, а высвобождаемая при этом каталаза расщепляет пероксид водорода, что также дает реакционноспособные кислородные частицы. Таким образом, полученная конструкция E.coli/BPQDs помогает поддерживать высокий уровень АФК вблизи злокачественной опухоли и повышает общую эффективность фотодинамической терапии. Отметим, однако, что бактериальные биогибридные материалы, образованные за счет сил электростатического взаимодействия, могут не обладать достаточной физиологической прочностью для применения in vivo. В некоторой степени эту проблему могла бы решить стратегия послойной самосборки модифицирующих компонентов на поверхности бактерии. Так, в работе [54] пробиотический штамм Bacillus coagulans был успешно инкапсулирован в оболочку из двух биоразлагаемых полисахаридов, хитозана и альгината, для защиты бактерии в кишечнике. Чередующиеся слои катионного полисахарида хитозана и анионного полисахарида альгината последовательно фиксировались на поверхности бациллы силами электростатического притяжения, формируя оболочку толщиной до трех бислоев (рис. 4). Интересное решение представлено в работе [67], где нанопластины слоистых двойных кобальт-медь-молибденовых гидроксидов (CoCuMo-LDH, layered double hydroxides) были прочно зафиксированы электростатически на бактериальной мембране пробиотического штамма Lactobacillus acidophilus. В дальнейшем, при участии метаболитов лактобациллы, кристаллические нанопластины подвергались фазовому переходу в аморфное состояние, характеризующееся более высокими фотодинамическими характеристиками.
2. БАКТЕРИЯ-РОБОТ СПЕШИТ НА ПОМОЩЬ: УПРАВЛЕНИЕ И ДОСТАВКА Эффективная доставка лекарств в область злокачественного новообразования и метастазов является одной из самых значительных проблем в терапии онкологий. Особенно это касается лечения солидных опухолей, расположенных в труднодоступных участках человеческого тела, для которых характерна низкая эффективность пассивной внутривенной доставки и ограниченный внутриопухолевый транспорт. По сравнению с нормальной тканью, сосудистая система опухоли хаотична, а расстояние между капиллярами велико, поэтому лишь незначительная доля (часто менее 1%) внутривенно введенного препарата попадает внутрь опухоли [68-69]. Известно, что терапевтические агенты размером менее ~5 нм (все низкомолекулярные лекарственные препараты) подвержены почечной фильтрации и клиренсу, что требует более высоких исходных концентраций, а следовательно, сопряжено с риском побочных эффектов. В то же время, терапевтические средства размером более 100 нм плохо проникают сквозь крошечные поры сосудистой сети [4]. Проблема неэффективной доставки усугубляется быстрым ростом раковых клеток и наличием плотного внеклеточного матрикса, что, в совокупности с отсутствием лимфатического дренажа, еще больше затрудняет транспорт медикаментов. Миниатюрный робот, снабженный терапевтическим агентом и способный самостоятельно передвигаться по направлению к опухоли и внутри нее, мог бы помочь решить эту проблему. Принципиальным преимуществом живых бактерий, на базе которых может быть сконструирован такой робот, является подвижность, помогающая им активно выбираться из сосудистой системы и проникать в опухолевые ткани [70]. Другая ключевая особенность бактерий – их независимость, то есть способность автономно существовать и выживать в сложных физиологических условиях, по крайней мере, в течение некоторого времени. Тем не менее, на пути к опухоли бактерии приходится непросто: в долгом путешествии по организму ей предстоит уклоняться от иммунных атак и преодолевать многочисленные барьеры, прежде чем проникнуть внутрь опухоли и запустить процесс высвобождения терапевтического агента (таблица 2).
2.1. Движение в сторону опухоли.
Хорошо известно, что некоторые виды анаэробных микроорганизмов – строго анаэробные клостридии и бифидобактерии или факультативно анаэробные сальмонеллы, листерии и E. coli, - попав в кровоток, достигают опухоли и избирательно колонизируют ее гипоксические и некротические очаги [71]. Для примера, в одной из ранних работ было продемонстрировано, что заражение мышей - носителей меланомы внутрибрюшинным введением штамма S. typhimurium дикого типа (ATCC 14028) приводит к накоплению бактерии внутри опухоли в количестве, превышающем 109 колоний-образующих единиц (КОЕ) на грамм опухолевой ткани [72]. Дополнительным фактором, привлекающим бактерии в зону опухоли, является иммунодефицитное микроокружение новообразования, помогающее микроорганизмам избежать атак иммунной системы, и хемотаксические продукты распада тканей [73]. Движение бактерии с кровотоком может происходить либо пассивно с постепенным накоплением в очагах опухоли, либо более активно - например, при помощи жгутиков. Жгутики бактерий вращаются подобно пропеллеру и могут помочь развить скорость плавания до 300 мкм/с [4]. Есть основания надеяться, что снабжение бактерии полезным терапевтическим грузом не изменит физиологические характеристики микроорганизма и скорость его передвижения настолько, чтобы стать серьезным препятствием для продвижения биологического робота и проникновения внутрь очагов новообразования. Действительно, по крайней мере на уровне клеточных моделей [74], в том числе пространственных [75], продемонстрировано, что конъюгация наноразмерных частиц-контейнеров с штаммом S. typhimurium не препятствует внутриопухолевому транспорту бактерии, при этом концентрация доставленного при помощи бактериобота препарата почти в 100 раз превышает объем терапевтического груза, проникающего внутрь опухоли благодаря пассивной диффузии [75]. В изотропной среде, в отсутствие аттрактантов, бактерия движется ненаправленно и хаотически. Как упоминалось выше, некоторую направленность движению бактерии, а следовательно, и бактериобота на ее основе, придает хемотаксис в сторону очагов некроза опухолевых тканей [37]. Привлекательной выглядит идея использовать внешние силы для стимуляции движения бактериального робота в желаемом направлении. Популярным и стремительно развивающимся подходом является использование магнитных полей для направления бактериобота от места введения в организм до места локализации опухоли [76-77]. В этом случае бактерия или бактериальный робот должны быть чувствительны к магнитным полям – как, например, магнитотаксическая Magnetococcus marinus (MC-1) - грам-отрицательный кокк, обитающий в Атлантическом океане [52]. Магнитосомы этой бактерии представляют собой частицы магнетита (Fe3O4), окруженные мембранами и образующие цепочки в цитозоле. Управление при помощи внешнего магнитного поля перитуморально введенным живым мышам биогибридом на основе МС-1, конъюгированного с нагруженными лекарственным средством нанолипосомами, приводит к значительному (до 55%) проникновению MC-1 в гипоксические регионы колоректальной опухоли; при этом у мышей не наблюдается явных признаков лихорадки или токсикоза вследствие введения чужеродного микроорганизма [78]. Помимо M. marinus, еще по крайней мере несколько видов природно магнитотропных бактерий находятся в активной разработке, в том числе Magnetovibrio MV-1 и представители рода Magnetospirillum – M. gryphiswaldense MSR-1, M. magneticum AMB-1 и M. magnetotacticum MS-1 [76]. Также можно придать свойство магниточувствительности бактерии, изначально этим свойством не обладавшей. В работе Aubry и соавторов [79] сконструирована кишечная палочка, стимулирующая образование богатых железом телец внутри клетки за счет сверхэкспрессии гена белка ферритина в процессе роста в обогащенной железистыми соединениями среде. По данным других авторов [57], чувствительность конструкции на основе E. coli к внешним полям была достигнута прикреплением магнитных наночастиц к бактериальной стенке. Биогибрид также включал нанолипосомы, нагруженные доксорубицином и фототермическим агентом, и был способен перемещаться под действием магнитного поля внутри биологических матриц, эффективно колонизировать опухолевые сфероиды и высвобождать терапевтический агент при воздействии инфракрасного излучения. "Гибридный" микроробот на основе аттеньюированного штамма S. typhimurium был создан в работе [80]. Магнитные наночастицы (Fe3O4) были заключены в альгинат-хитозановую биоразлагаемую капсулу и прикреплены электростатически к бактериальной стенке сальмонеллы. Испытания в гелевой микрофлюидной модельной системе подтвердили способность сконструированного биогибрида двигаться под действием электромагнитного поля в кровотоке крупных сосудов даже против течения, в то время как в более мелких сосудах и внутри тканей передвижение контролировалось работой бактериальных жгутиков и хемотаксисом. 2.2. Нацеливание и распознавание.Движение бактериального робота к мишени-опухоли может быть дополнительно искусственно стимулировано. Как правило, усиление тропности бактериобота к опухоли связано с генетической модификацией его основного несущего элемента - бактерии. В результате мутаций и других генетических/эпигенетических отклонений раковые клетки и их микроокружение приобретают химические и физические характеристики, которые отличаются от характеристик здоровых клеток. В частности, раковые клетки продуцируют аномальные белки клеточной поверхности - неоантигены, которые являются специфическими для опухоли и, таким образом, представляют собой уникальные мишени [81]. Генетическая модификация бактерии может помочь вывести на ее поверхность специфичные для опухоли лиганды. Park и соавторы [82] разработали штамм S. typhimurium SHJ2037 (ΔppGpp-дефицитный), со свойством отображать пептидный фрагмент RGD (ACDCRGDCFCG) на наружной петле внешнемембранного белка OmpA. Фрагмент RGD связывается с интегрином avβ3, избыточно продуцируемым раковыми клетками, и, таким образом, бактериальный штамм может быть точно нацелен на растущую опухоль. Действительно, штамм SHJ2037 продемонстрировал высокую опухолевую специфичность и значительный терапевтический эффект в отношении рака молочной железы и рака кожи. Опухолевая специфичность сальмонеллы также может быть усилена с помощью синтеза на поверхности бактерии однодоменного антитела (VHH), направленного на ассоциированный с опухолью антиген (hCD20) [83]. Антителозависимое нацеливание определяло эффективность инфицирования CD20+ клеток лимфомы in vitro и in vivo при значительном снижении неспецифической клеточной инвазии. Другой подход - экспозиция на клеточной стенке бактерии синтетических адгезинов, повышающих специфичность бактериальной адгезии к раковым клеткам [71]. Сконструированные адгезины имеют модульную структуру - цилиндрический бета-домен поверхностного белка интимина заякорен в бактериальной мембране и держит иммуноглобулиноподобный (Ig) адгезивный VHH-домен, - и могут быть легко модифицированы под интересующий тип опухоли заменой VHH-последовательности. Непатогенные штаммы E. coli, снабженные такими адгезинами, более успешно колонизировали солидные опухоли, экспрессирующие ген таргетного антигена, в сравнении с кишечной палочкой дикого типа. Некоторые соединения в микроокружении опухоли могут выступать как природные хемоаттрактанты для бактерий - как, например, сверхпродуцируемый раковыми клетками фактор роста эндотелия сосудов (VEGF), привлекающий непатогенные штаммы E. coli [84]. Нацеливание на область новообразования может также быть усилено конструкцией нутриент-дефицитных штаммов, которые могли бы добывать необходимые вещества (например, аминокислоты) из микроокружения опухоли. Так, штамм S. typhimurium A1-R, ауксотрофный по лейцину и аргинину, продемонстрировал впечатляющую терапевтическую эффективность, приводя к замедлению роста опухоли в сравнении с контролем в мышиных моделях рака простаты, молочных желез, поджелудочной железы и яичников, так же как сарком и глиом различной этиологии [85]. 2.3. Проникновение внутрь раковых клеток.В некоторых случаях наиболее выигрышной стратегией было бы проникновение бактериального курьера непосредственно внутрь раковой клетки, для последующего высвобождения терапевтического груза. Для проникновения в опухолевую клетку бактерия может быть снабжена "модулем инвазии", состоящим из конститутивно экспрессируемого гена белка инвазина (inv) Yersinia pseudotuberculosis. Инвазин связывается с β1-интегринами, сверхпродуцируемыми на поверхности клеток-мишеней в различных видах опухолей, и провоцирует захват бактерии посредством фагоцитоза [86] (Рис. 5). Помимо локуса inv, генно-инженерная конструкция предполагает также наличие гена hlyA из Listeria monocytogenes, который кодирует цитолизин, помогающий разрушить фагосомальную мембрану и выпустить терапевтический агент в цитоплазму. Такая стратегия была использована в работе [87] для доставки загруженных в непатогенный штамм E. coli трансгенных интерференционных РНК против онкогенного белка HPV16-E7 в клетки плоскоклеточного рака полости рта.
Как упоминалось выше, в солидных опухолях бактерии могут мигрировать внутрь некротических участков благодаря гипоксическому тропизму и хемотаксису, а иммуносупрессивная среда создает благоприятные условия для размножения. Быстро растущее число бактерий активирует иммунную систему хозяина в зоне опухоли и привлекает иммунные клетки. Однако, чтобы достичь опухолей, находящихся зачастую в тех отделах человеческого тела, которые в норме считаются стерильными (кровь, легкие, мочевой пузырь, печень, костная ткань и т.п.), бактериальному роботу необходимо преодолеть иммунную защиту макроорганизма в кровеносных сосудах и нормальных тканях. Бактерия, даже лишенная возможности размножаться, является чужеродным и токсичным для макроорганизма элементом, что ставит под вопрос эффективность доставки терапевтического груза. Одним из способов обойти иммуногенность и токсичность живых «курьеров» является генетическое нокаутирование иммуногенных элементов бактериальных мембран; однако эта стратегия может привести к значительному ослаблению штамма и снижению эффективности колонизации [88-91]. Альтернативный вариант – маскировка микробных поверхностей неиммуногенными молекулами, такими как упомянутые в предыдущем разделе альгинат-хитозановые покрытия [54, 92], полидофамин [93], биосовместимые липиды [94] или полимерные наночастицы [95]. Интересный вариант нейтрализации взаимного влияния бактериобота и макроорганизма, основанный на программируемой инкапсуляции бактериальной клетки, предложен в работе Harimoto и соавторов [96]. Авторы этого исследования модифицировали штамм кишечной палочки E. coli Nissle 1917 таким образом, чтобы он был способен контролировать экспрессию генов капсульных полисахаридов при помощи внешнего индуктора, в качестве которого выступал ИПТГ (изопропил-β-D-1-тиогалактопиранозид). Регулируемый и динамический синтез полисахаридной капсулы обеспечивал временную защиту бактерий от иммунных атак при перемещении к опухоли, в то время как потеря капсулы приводила к эффективному устранению микроорганизма после завершения его миссии. 3. ВООРУЖЕННЫЙ ДО ЗУБОВ: ТЕРАПЕВТИЧЕСКИЙ И ДИАГНОСТИЧЕСКИЙ ПОТЕНЦИАЛ БАКТЕРИАЛЬНОГО РОБОТА Среди других, важнейшая характеристика бактериального микроробота – это условный «груз», который он может доставить. Условный – потому что сама бактерия может играть роль не только переносчика разнообразных терапевтических молекул, но и «живого снаряда», несущего на своей поверхности иммуногенные компоненты, или мобильной фабрики для производства лекарств или пролекарств непосредственно в зоне опухоли. Как неоднократно упоминалось, бактерии способны стимулировать мощный иммунный ответ в зоне опухоли, привлекая и активируя иммунные клетки в ее микроокружение, и обеспечивая противоопухолевый эффект. Помимо заложенных природой факторов иммуногенности, к числу которых относятся пептидогликан, липополисахариды, липотейхоевые кислоты и др., генно-модифицированные бактерии могут также вырабатывать дополнительные иммуномодулирующие компоненты, направленные на стимуляцию иммуносупрессивной среды опухоли [47, 97-99]. Например, терапевтический штамм на основе непатогенного штамма E. coli Nissle 1917, сконструированный в работе Leventhal и соавторов, экспрессирует циклический диаденинмонофосфат (cyclic diAMP, CDA) для активации одного из иммунных сигнальных путей – STING [100]. Естественный метаболизм бактерии также может быть направлен против опухоли, поскольку размножающиеся бактерии конкурируют с раковыми клетками за питательные вещества, могут изменять рН среды микроокружения опухоли или продуцировать специфические метаболиты, угнетающие рост опухолевых клеток – токсины, АФК и т.п. [88, 101-102]. Эти свойства могут быть дополнительно усилены в генно-модифицированных штаммах. Бактерия, достигшая опухоли, может служить источником непрерывного экспорта миРНК для "выключения" генов, связанных с размножением опухолевых клеток, в РНК-интерференционной терапии. Пример такого подхода - аттенуированный штамм S. typhimurium, несущий плазмиду с короткой шпилечной РНК для подавления экспрессии опухолевыми клетками PD-L1 - лиганда белка программируемой клеточной гибели, участвующего в механизмах ускользания от иммунного контроля [103]. В комбинации с лучевой терапией, этот метод позволил достичь значительного ингибирования пролиферации опухолевых клеток. Как естественные микрофабрики белка, бактерии могут производить и секретировать в зоне опухоли антитела, ферменты, факторы воспаления, белки, блокирующие или модулирующие метаболизм, или индукторы апоптоза. В рамках еще одного известного подхода бактерия может кодировать фермент, катализирующий превращение пролекарства в фармакологически активное противоопухолевое соединение. Преимущество такого подхода заключается в том, что активный препарат может обладать высокой токсичностью, введение же его в организм в форме пролекарства снижает риск побочных эффектов. Наконец, бактерия может служить курьером, доставляющим контейнер с противоопухолевым агентом [5, 104-106]. Надо сказать, что в попытках сделать из бактерии универсальное высокоэффективное оружие исследователи проявляют удивительную изобретательность. Тенденция последнего времени – стремление сконструировать бактериального робота многофункциональным, наделить его комбинацией различных терапевтических и диагностических инструментов: так, один бактериобот может сочетать возможности иммунотерапии с химиотерапией или с преимуществами таких подходов, как радиотерапия (РТ), фототермическая (ФТТ) или фотодинамическая (ФДТ) терапия [91, 107-109]. Например, сложный и красивый образец многофункционального (мультимодального) бактериального биогибрида, сочетающего возможности химиотерапии с метаболической бактериальной терапией, представлен в работе [110], где непатогенный штамм S. oneidensis MR-1 был снабжен "контейнерами" металлоорганического каркаса MIL-101-MOF, нагруженными доксорубицином. Род Shewanella относится к электрогенным, то есть обладает способностью участвовать в процессах переноса электронов, также штамм MR-1 селективно метаболизирует молочную кислоту в качестве источника энергии. Утилизация избыточного количества лактата в зоне опухоли позволяет улучшить результаты химиотерапии, при этом происходит восстановление катиона железа Fe3+ - ключевого элемента металлоорганического каркаса - до Fe2+, что, в свою очередь, приводит к деградации MIL-101-MOF и высвобождению доксорубицина. Катионы Fe2+ могут далее взаимодействовать с пероксидом водорода в зоне опухоли с формированием гидроксил-радикалов, которые также оказывают повреждающее действие на клетки, а образующиеся ионы Fe3+ принимают дальнейшее участие в катаболизме лактата. Больше примеров мультимодальных бактериоботов можно найти в прекрасных обзорах последних лет [107, 111-115], и в Таблице 1. 4. БЕЗОПАСНОСТЬ Одна из важнейших сторон концепции создания биологического робота для контролируемой доставки терапевтических агентов – вопрос о биобезопасности, который подразумевает, помимо безопасности для человека, множество других аспектов, в том числе нетоксичность для окружающей среды и способность к деградации и утилизации после завершения миссии. Значительное внимание уделяется биосовместимости, направленной на минимизацию последствий долговременного пребывания в организме хозяина и снижение воздействия на нормальные ткани. Наибольшую озабоченность, как правило, вызывает основной конструктивный элемент бактериобота – бактерия. Бактерии способны неконтролируемо размножаться внутри макроорганизма, запускать инфекционный процесс и продуцировать токсичные для тканей вещества. Даже в том случае, если бактерия нежизнеспособна или лишена возможности размножаться, угрозу может представлять ее ДНК, вследствие возможного переноса генетического материала в близкородственные штаммы, населяющие микробиом человека. Одной из стратегий "биологического сдерживания" является создание ауксотрофных штаммов. Данный подход предполагает удаление из генома бактерии гена, кодирующего важный для ее существования метаболит, таким образом жизнеспособность бактерии оказывается ограниченной теми регионами, где необходимый компонент может быть получен извне [116]. Так, штамм SYNB1891 на основе E coli Nissle 1917, ауксотрофный по тимидину и диаминопимелиновой кислоте в результате удаления, соответственно, генов thyA и dapA, был сконструирован в работе [100] как прототип противоопухолевого средства. Диаминопимелиновая кислота - компонент клеточной стенки грамотрицательных бактерий - отсутствует в метаболизме эукариот, поэтому ауксотрофный по данному соединению бактериальный штамм не смог бы долго выживать в тканях млекопитающих. Тимидин, дефицит которого обычно наблюдается во внеклеточных средах, также может быть рассмотрен как эффективный инструмент управления поведением бактерии. Очевидным требованием контроля биологической безопасности представляется чувствительность бактерии-робота к антибиотикам. Чтобы исключить развитие резистентности в процессе пребывания бактерии в человеческом организме, гены или генные кассеты устойчивости к антимикробным препаратам могут быть предварительно удалены или заблокированы, как это было сделано, например, в упомянутой выше работе [100]. В перечне способов контроля над популяцией бактерий в организме хозяина рассматривается также использование индуцируемых внешним сигналом суицидных генов [104] или предложенный в работе Chan и соавторов [117] «контроллер аварийного отключения» («deadman kill switch») бактерии - генно-инженерная система защиты на уровне транскрипции, связывающая определенные сигналы окружающей среды с подавлением или, наоборот, стимуляцией выработки смертельного для бактериальных клеток токсина. Еще один подход к обеспечению безопасности терапевтических средств на основе микроорганизмов - разработка бактерий с минимальным (редуцированным) геномом. Данный метод предполагает удаление из генома кодирующих последовательностей, не являющихся необходимыми для существования бактерии. Минимальный геном содержит только те гены, которые требуются для поддержания жизнедеятельности микроорганизма, и практически исключает возможность адаптации бактерии к изменяющимся условиям окружающей среды [118]. 5. БАКТЕРИАЛЬНЫЙ РОБОТ... БЕЗ БАКТЕРИИ: ПЕРСПЕКТИВЫ Для создания бактериального робота можно использовать не всю бактерию целиком, а лишь ее части или структурные компоненты. Такой подход позволяет повысить безопасность терапии без потери преимуществ использования биологического носителя. Так, широко исследовался потенциал бактериальных мини-клеток, мембранных везикул, магнитосом, «бактериальных призраков» или спор. Бактериальные мини-клетки представляют собой наноразмерные (диаметром 100-400 нм), неживые, безъядерные, неделящиеся клетки, которые образуются в результате мутаций в генах minCDE [119]. Эти мутации приводят к нарушениям в формировании септы, вследствие чего септа оказывается в клетке не единичной или же расположенной не по центру, а ближе к полюсам. Мини-клетки содержат все компоненты родительской клетки, за исключением хромосомной ДНК. Несмотря на то, что мини-клетки не могут размножаться, они сохраняют остаточную метаболическую активность. Основным преимуществом мини-клеток считается их способность эффективно инкапсулировать внутри себя лекарственное средство: так, одна мини-клетка может вместить до миллиона молекул доксорубицина, это примерно в сто раз больше, чем объем загрузки липосомы [119]. Бактериальный призрак (bacterial ghost) - это, по сути, пустая оболочка бактериальной клетки, преимущественно грамотрицательных видов. Она лишена цитоплазматических компонентов, но сохраняет мембрану с полным набором антигенных белковых структур [120]. Такие подобия бактерий могут быть получены в результате экспрессии гена Е бактериофага øX174 внутри клетки-мишени, при этом продуцируется белок-лизин, который формирует трансмембранный туннель диаметром до 200 нм, что приводит к истечению содержимого цитоплазмы из-за разницы осмотического давления внутри и снаружи клеточной оболочки. Подобные структуры – мини-клетки и бактериальные призраки – сходны тем, что не имеют возможности размножаться и активно метаболизировать, однако сохраняют, полностью или частично, морфологию клеток и антигенные элементы поверхности – мембранные белки, адгезины, липополисахариды и пептидогликаны. Более того, такие структуры, как и живые бактерии, могут быть дополнительно модифицированы для лучшего нацеливания на раковые клетки, в то время как пустое пространство внутри клеточных оболочек может быть использовано для размещения полезного терапевтического груза. Активно изучаются бактериальные внешнемембранные везикулы (Outer Membrane Vesicles, OMV) - наноразмерные (20-300 нм) сферические двуслойные липосомы, сформированные из фрагментов внешней мембраны и клеточной стенки грамотрицательных бактерий [121]. При отсутствии вирулентности в сравнении с живой бактерией, OMV обладают высокой иммуногенностью и способны стимулировать естественный иммунитет. Помимо этого, OMV могут проникать в клетку-мишень хозяина путем слияния с клеточной мембраной или посредством эндоцитоза, таким образом повышая эффективность доставки лекарств [121]. Привлекательной представляется и возможность использовать споры бактерий для доставки терапевтических средств в зону опухоли. Бактериальные споры, которые, по сути, представляют собой гарантию выживания вида в неблагоприятных условиях окружающей среды, крайне устойчивы к механическим или химическим воздействиям и колебаниям температуры, и, таким образом, имеют мощный потенциал для использования в качестве курьеров – доставщиков лекарственных средств внутри человеческого организма. В гипоксических очагах опухоли споры анаэробных бактерий могут прорастать в вегетативное состояние для синтеза и секреции терапевтических белков [122]. В предыдущих главах упоминались магнитотаксические бактерии, способные синтезировать внутри собственной клетки уникальные органеллы - магнитосомы. Магнитосомы представляют собой кристаллы оксида или сульфида железа, окруженные фосфолипидной мембраной. Эти органеллы могут быть выделены из бактериальных клеток и использованы в терапии онкологий для направленной доставки лекарственных средств под действием магнитного поля [123]. Отдельные примеры, иллюстрирующие потенциал различных биологических носителей бактериальной природы, приведены в таблице 3.
ЗАКЛЮЧЕНИЕ Бактерии являются постоянными спутниками человеческого тела на протяжении всей жизни человека и даже после его смерти. Эти крошечные, невидимые невооруженным глазом живые существа в ходе эволюции научились сосуществовать с человеческим организмом и выработали множество различных инструментов для взаимодействия с ним. Поэтому идея создания управляемых роботов на основе бактерий, способных свободно ориентироваться и передвигаться внутри тела человека, представляется многообещающей. Однако, несмотря на многочисленные исследования и определенный прогресс, применение такого рода терапии в клинической практике все еще не стало рутинным. Основная проблема заключается в необходимости сделать поведение бактерий абсолютно предсказуемым, а также обеспечить надежный контроль над безопасностью и эффективностью этого потенциально мощного терапевтического инструмента. Тем не менее, последние годы характеризуются значительным продвижением на пути превращения природной бактерии в идеального медицинского микроробота с заданными свойствами. Отдельные генно-модифицированные бактериальные штаммы в настоящее время проходят последние этапы клинических исследований, предваряющих регистрацию лекарственных препаратов в терапии онкозаболеваний [8, 31, 47, 91, 97, 107]. Основным - и существенным - преимуществом бактериобота, в сравнении с рутинными подходами, можно считать возможность соединить в одном миниатюрном устройстве различные способы воздействия на опухолевую ткань, и обеспечить, таким образом, комплексную стратегию лечения рака. Разработка и изготовление бактериальных микророботов – непростая задача, требующая интеграции технологий из разных областей исследований, таких как микробиология, генетическая инженерия, нано- и биотехнологии, синтетическая биология и микрофлюидика, а также привлечения возможностей искусственного интеллекта для прогнозирования свойств, и клинической медицины для оценки результата. В отдельных работах [86, 104] бактерию и биогибриды на ее основе предлагают рассматривать как совокупность уникальных модулей, каждый из которых выполняет свою, строго установленную, функцию, при этом характеристики каждого из модулей могут быть при необходимости трансформированы под различные задачи. В заключение, стоит отметить, что при достаточно большом количестве лабораторных прототипов, до реального рутинного применения бактериальных биогибридов в клинической практике все еще достаточно долгий путь - путь, на котором предстоит ответить в том числе на множество вопросов, которые сейчас освещены достаточно слабо, например, вопросы фармакокинетики и фармакодинамики препарата в человеческом организме. Но этот путь определенно имеет перспективы. СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ Настоящая статья не содержит каких-либо исследований с участием людей или с использованием животных в качестве объектов. БЛАГОДАРНОСТИ Автор признателен О.Л. Курбатовой за неоценимую помощь с оформлением рисунков к статье и Л.К. Курбатову за плодотворные дискуссии и полезные замечания. ФИНАНСИРОВАНИЕ Работа выполнена в отсутствие внешнего финансирования. КОНФЛИКТ ИНТЕРЕСОВ Авторы заявляют об отсутствии конфликта интересов. ЛИТЕРАТУРА
|