ПОСЛЕДОВАТЕЛЬНОСТЬ, ДОПОЛНЯЮЩАЯ КОРОВУЮ ПОСЛЕДОВАТЕЛЬНОСТЬ ПРОМОТОРА T7 С 3′-КОНЦА, В КОНСТРУИРОВАНИИ NASBA-ПРАЙМЕРОВ: ВЛИЯНИЕ НА ЭФФЕКТИВНОСТЬ АМПЛИФИКАЦИИ
1Научно-исследовательский институт биомедицинской химии им. В.Н. Ореховича, 119121, Москва, Погодинская ул., 10; e-mail: khmelevaswetlana@yandex.ru
2Химический факультет Московского государственного унивеситета им. М.В.Ломоносова, Россия, 119991, Москва, Ленинские горы, 1/3
Ключевые слова: NASBA, промотер T7, конструирование праймеров, эффективность амплификации
DOI:10.18097/BMCRM00302
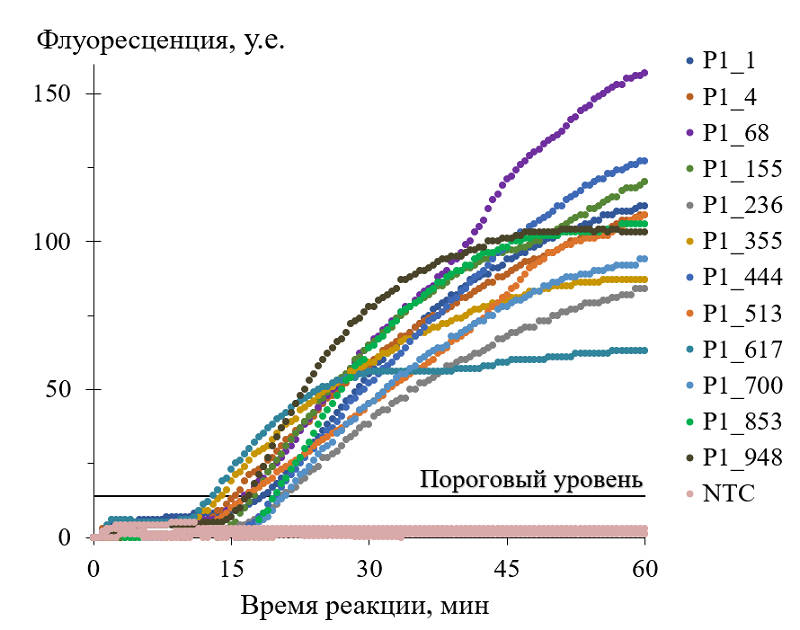
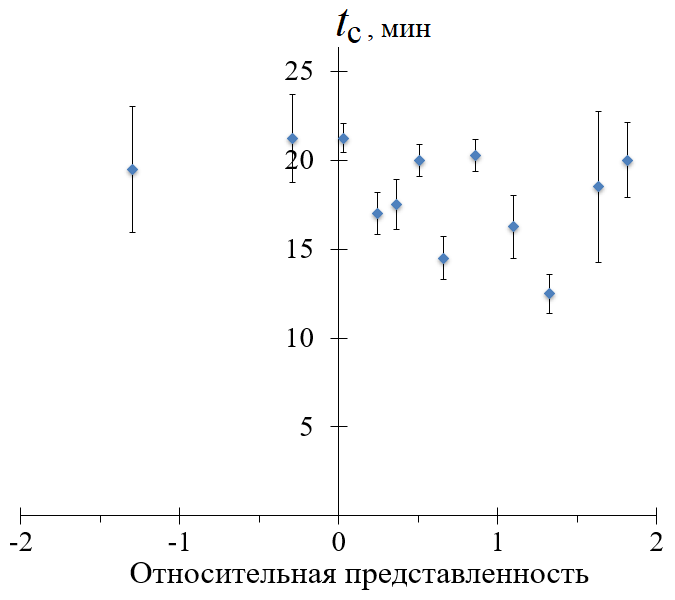
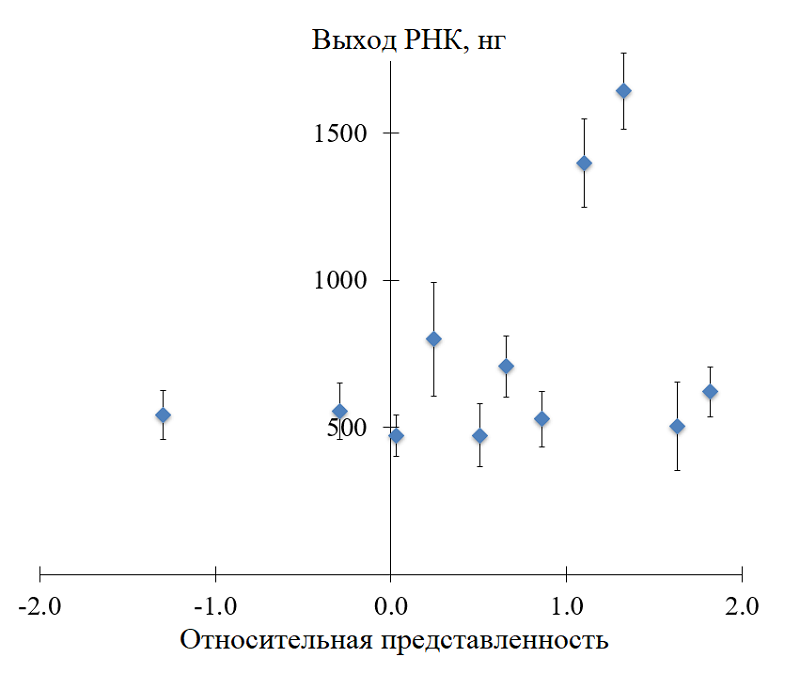
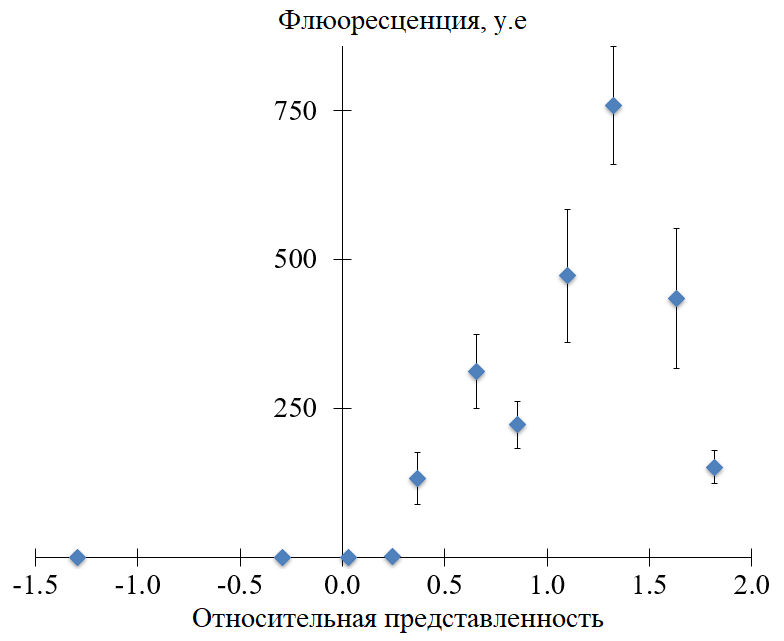
NASBA (Nucleic Acid Sequence Based Amplification) – метод изотермической амплификации РНК, позволяющиq выявлять инфекционные агенты в лабораторных внелабораторных условиях. Он основан на присутствии промотора РНК-полимеразы фага T7 в одном из праймеров NASBA, и эффективность метода в значительной степени зависит от силы промотора. Известно, что при транскрипции in vitro сила промотора в значительной степени зависит от последовательности, расположенной непосредственно после коровой последовательности промотора T7. В данной работе эффективность NASBA была экспериментально оценена для различных вариантов 8-нуклеотидных последовательности, расположенной непосредственно после коровой последовательности промотора T7. Варианты были ранжированы по известным выходам РНК, образующейся при транскрипции in vitro. Было обнаружено, что ранг 8-нуклеотидного продления основной последовательности промотора T7 может служить основанием для рационального выбора последовательнойтей эффективных праймеров NASBA. При этом не все 8-нуклеотидные продления, характеризующиеся наибольшим выходом РНК при транскрипции in vitro, обеспечивают наиболее эффективную амплификацию РНК-мишеней в NASBA. Для выбора наилучших кандидатов в праймеры NASBA по-прежнему требуется тщательная оценка способности праймера образовывать вторичные структуры с использованием алгоритмов сворачивания ДНК.
|
ЗАКРЫТЬ

|
Таблица 1.
Варианты праймера Р1, использованные в работе. Коровая последовательность промотора Т7 выделена синим шрифтом. Последовательность нуклеотидной вставки, влияющей на эффективность праймера в NASBA, выделена красным.
|
ФИНАНСИРОВАНИЕ
Работа выполнена в рамках Программы фундаментальных научных исследований в Российской Федерации на долгосрочный период (2021 - 2030 годы) (№ 122030100170-5).
- Bodulev, O.L., Sakharov, I.Y. (2020) Isothermal Nucleic Acid Amplification Techniques and Their Use in Bioanalysis. Biochemistry (Moscow), 85, 147–166. DOI
- Zhao, Y., Chen, F., Li, Q., Wang, L., Fan, C. (2015) Isothermal Amplification of Nucleic Acids. Chem. Rev., 115, 12491–12545. DOI
- Abel, G. (2015) Current status and future prospects of point-of-care testing around the globe. Expert Review of Molecular Diagnostics, 15, 853–855. DOI
- Hu, B., Guo, H., Si, H., Shi, Z. (2024) Emergence of SARS and COVID-19 and preparedness for the next emerging disease X. Frontiers in Medicine, 18, 1–18. DOI
- Yang, H., Ledesma-Amaro, R., Gao, H., Ren, Y., Deng, R. (2023) CRISPRbased biosensors for pathogenic biosafety. Biosensors and Bioelectronics, 228, 115189. DOI
- De Felice, M., De Falco, M., Zappi, D., Antonacci, A., Scognamiglio, V. (2022) Isothermal amplification-assisted diagnostics for COVID-19. Biosensors and Bioelectronics, 205, 114101. DOI
- Fernandes, R.S., De Oliveira Silva, J., Gomes, K.B., Azevedo, R.B., Townsend, D.M., De Paula Sabino, A., Branco De Barros, A.L. (2022) Recent advances in point of care testing for COVID-19 detection. Biomedicine and Pharmacotherapy, 153, 113538. DOI
- Deiman, B., van Aarle, P., Sillekens, P. (2002) Characteristics and applications of nucleic acid sequence-based amplification (NASBA). Molecular Biotechnology, 20, 163-179. DOI
- Honsvall, B.K., Robertson, L.J. (2017) From research lab to standard environmental analysis tool: Will NASBA make the leap? Water Resources, 109, 389-397. DOI
- Compton, J. (1991) Nucleic acid sequence-based amplification. Nature, 350, 91–92. DOI
- Tang, G.Q., Bandwar, R.P., Patel, S.S. (2005) Extended upstream A-T sequence increases T7 promoter strength. Journal of Biological Chemistry, 280, 40707-40713. DOI
- Romano, J.W., Williams, K.G., Shurtliff, R.N., Ginocchio, C., Kaplan, M. (1997) NASBA technology: isothermal RNA amplification in qualitative and quantitative diagnostics. Immunological Investigations, 26, 15–28. DOI
- Ju, Y., Kim, H.Y., Ahn, J.K., Park, H.G. (2021) Ultrasensitive version of nucleic acid sequence-based amplification (NASBA) utilizing a nicking and extension chain reaction system. Nanoscale, 13, 10785–10791. DOI
- Guoshuai, J., Xiaomeng, X., Zengdan, G., Xingxing, H., Qi, P., Hanbing, Z., Yi, W. (2022) A rapid and high sensitivity RNA detection based on NASBA and G4-ThT fluorescent biosensor. Scientific Reports, 12, 10076. DOI
- Lu, X., Shi, X., Wu, G., Wu, T., Qin, R., Wang, Y. (2017) Visual detection and differentiation of Classic Swine Fever Virus strains using nucleic acid sequencebased amplification (NASBA) and G-quadruplex DNAzyme assay. Scientific Reports, 7, 44211. DOI
- Loeffler, J., Hebart, H., Cox, P., Flues, N., Schumacher, U., Einsele, H. (2001) Nucleic Acid Sequence-Based Amplification of Aspergillus RNA in Blood Samples. Journal of Clinical Microbiology, 39, 1626–1629. DOI
- Abd El Galil, K.H., El Sokkary, M.A., Kheira, S.M., Salazar, A.M., Yates, M.V., Chen, W., Mulchandani, A. (2005) Real-Time Nucleic Acid Sequence- Based Amplification Assay for Detection of Hepatitis A Virus. Applied and Environmental Microbiology, 71, 7113–7116. DOI
- Leone, G., van Schijndel, H.B., van Gemen, B., Schoen, C.D. (1997) Direct detection of potato leafroll virus in potato tubers by immunocapture and the isothermal nucleic acid amplification method NASBA. The Journal of Virological Methods, 66, 19–27. DOI
- Aufdembrink, L.M., Khan, P., Gaut, N.J., Adamala, K.P., Engelhart, A.E. (2020) Highly specific, multiplexed isothermal pathogen detection with fluorescent aptamer readout. RNA, 26, 1283–1290. DOI
- Wang, Jiasi, Kreutz, J.E., Thompson, A.M., Qin, Y., Sheen, A.M., Wang, Jingang, Wu, L., Xu, S., Chang, M., Raugi, D.N., Smith, R.A., Gottlieb, G.S., Chiu, D.T. (2018) SD-chip enabled quantitative detection of HIV RNA using digital nucleic acid sequence-based amplification (dNASBA). Lab on a Chip, 18, 3501–3506. DOI
- Cools, I., Uyttendaele, M., D’Haese, E., Nelis, H.J., Debevere, J., 2006. Development of a real-time NASBA assay for the detection of Campylobacter jejuni cells. Journal of Microbiological Methods 66, 313–320. https://doi. org/10.1016/j.mimet.2005.12.004
- Wu, Q., Suo, C., Brown, T., Wang, T., Teichmann, S., Bassett, A. (2020) INSIGHT: a scalable isothermal NASBA-based platform for COVID-19 diagnosis. BioRxiv, DOI
- Moll, P,R., Duschl, J., Richter, K. (2004) Optimized RNA amplification using T7-RNA-polymerase based in vitro transcription. Analytical Biochemistry, 334, 164-174. DOI
- Sari, Y., Sousa Rosa, S., Jeffries, J., Marques, M.P.C. (2024) Comprehensive evaluation of T7 promoter for enhanced yield and quality in mRNA production. Scientific Reports, 14, 9655. DOI
- Conrad, T., Plumbom, I., Alcobendas, M., Vidal, R., Sauer, S. (2020) Maximizing transcription of nucleic acids with efficient T7 promoters. Communications Biology, 3, 439. DOI
- Deich, C., Cash, B., Sato, W., Sharon, J., Aufdembrink, L., Gaut, N.J., Heili, J., Stokes, K., Engelhart, A.E., Adamala, K.P. (2023) T7Max transcription system. Journal of Biological Engineering, 17, 4. DOI
- Komura, R., Aoki, W., Motone, K., Satomura, A., Ueda, M. (2018) Highthroughput evaluation of T7 promoter variants using biased randomization and DNA barcoding. PLoS One, 13, e0196905. DOI
- van Beckhoven, J.R., Stead, D.E., van der Wolf, J.M. (2002) Detection of Clavibacter michiganensis subsp. sepedonicus by AmpliDet RNA, a new technology based on real time monitoring of NASBA amplicons with a molecular beacon. Journal of Applied Microbiology, 93, 840-849. DOI
- Khmeleva, S.A., Kurbatov, L.K., Ptitsyn, K.G., Timoshenko, O.S., Morozova, D.D., Suprun, E.V., Radko, S.P., Lisitsa, A.V. (2024) Detection of Potato Pathogen Clavibacter sepedonicus by CRISPR/Cas13a Analysis of NASBA Amplicons. International Journal of Molecular Sciences, 25, 12218. DOI